 |
| Eleftheria terrae, una betaproteobacteria productora del antibiótico teixobactina. Origen de la imagen: Science News |
 |
| Mecanismo de actuación de la teixobactina. Clikear para ampliar. A la izquierda se representa une esquema de la bacteria Gram negativa Eleftheria terrae secretando el antibiótico y éste uníéndose a las moléculas objetivo (rectángulo con la palabra TEIX). A la derecha tenemos una visión ampliada del mecanismo de acción sobre el lípido II y el lípido III que se encuentran localizados en la membrana plasmática. El interior celular estaría en la parte inferior y el exterior en la superior. En el esquema representan de manera simplificada los pasos de síntesis de los monómeros que formarán el peptidoglicano (hexágonos azules y verdes) y de los monómeros que formarán los ácidos teicoicos (elipses rojas y azules). También se muestra el sitio de unión de la vancomicina (rectángulo rojo), que aunque afecte a la misma molécula, lo hace en un lugar diferente. Fuente: Sci-news.com |
Pero hay otros factores a tener en cuenta para que una molécula que se descubre de una bacteria del suelo llegue hasta los estantes de las farmacias. Uno de los principales es la cantidad de antibiótico que se puede obtener de un cultivo del microorganismo productor. Y aquí había dos inconvenientes: el primero es que Eleftheria terrae no es precisamente un buen microorganismo industrial de fácil crecimiento, el segundo es que la teixobactina no era sencilla de purificar a partir de los cultivos de dicha bacteria.
Evidentemente más de un grupo se ha puesto a buscar formas de producir mayor cantidad del antibiótico. Una por ejemplo es clonar los genes responsables de la biosíntesis del antibiótico en otro microorganismo que sea mucho más fácil de crecer en condiciones industriales. Otros han buscado formas de purificar más eficientemente el antibiótico. Y finalmente hay otra forma: sintetizar la teixobactina de forma artificial.
La síntesis de antibióticos artificiales no es nueva. El cloranfenicol originariamente fue descrito como un antibiótico producido por Streptomyces venezuelae, pero ahora resulta mucho más barato producirlo enteramente mediante síntesis química. Quizás pueda suceder lo mismo con la teixobactina, aunque sea un depsipéptido macrocíclico algo complejo. De hecho, las primeras pruebas para sintetizar químicamente la teixobactina no funcionaron ya que uno de los aminoácidos precursores, la enduracidina, era muy difícil de obtener.
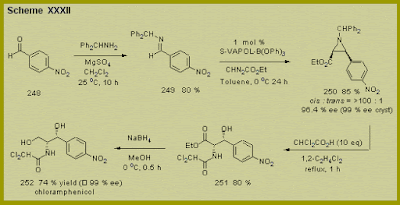 |
| Síntesis artificial del cloranfenicol. Fuente: Michigan State University |
Pero el grupo liderado por Ishwar Singh, de la Universidad de Lincoln en el Reino Unido ha encontrado que la enduracidina puede ser sustituida por otro tipo de aminoácidos, incluyendo aminoácidos apolares como la leucina o la valina. Lo que se obtiene no es exactamente la teixobactina natural ya que su composición química es distinta, pero las nuevas moléculas funcionan igual de bien frente a las bacterias. Pero las ventajas son evidentes. Los aminoácidos utilizados son muchísimo más baratos y esto permite pensar en que probablemente se establecerá una ruta de síntesis química para producir industrialmente los análogos de teixobactina. Eso permitirá que en breve se pueda pensar en diseñar ensayos clínicos con humanos.
 |
| Teixobactina natural (izquierda) y teixobactina sintética (derecha). En rojo se indican los D-aminoácidos y en negro los L. En azul se indica la posición de la enduracina en la teixobactina natural. En la artificial, dicho aminoácido se ha sustituido por la leucina. Fuente: Parmar et al. 2017. |
Además, este avance ha permitido entender en parte como puede ser el mecanismo de acción de la teixobactina. Hasta ahora se pensaba que los aminoácidos catiónicos que presenta eran los responsables de su actuación, pero los aminoácidos usados no están cargados, así que eso parece indicar que las cargas catiónicas no están involucradas en la unión al objetivo molecular. Una nueva vía de investigacións e abre.
No hay comentarios:
Publicar un comentario